Az elektrokémiai kettősréteg az elektrolit és az elektód határán alakul ki.
Amennyiben az elektódon egy adott felületi töltést ![]() helyezünk el, akkor az ellentétes töltésű ionokat ez az elektródtöltés az elektródhoz vonzza, míg az azonos töltésű ionokat inkább taszítja.
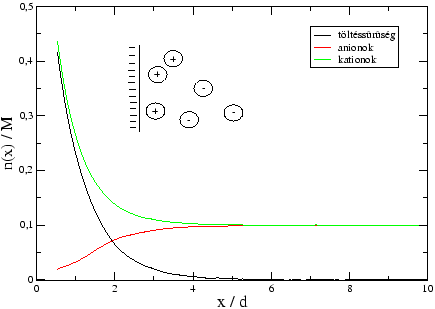
Ahogy az 1. ábra mutatja, ez egy valószínűségi kijelentés.
Ha feltesszük, hogy az elektródtöltés negatív, a kationok lokális sűrűsége nagyobb az elektród közelében mint az anionok sűrűsége,
helyezünk el, akkor az ellentétes töltésű ionokat ez az elektródtöltés az elektródhoz vonzza, míg az azonos töltésű ionokat inkább taszítja.
Ahogy az 1. ábra mutatja, ez egy valószínűségi kijelentés.
Ha feltesszük, hogy az elektródtöltés negatív, a kationok lokális sűrűsége nagyobb az elektród közelében mint az anionok sűrűsége, ![]() ill.
ill. ![]() , ahol
, ahol ![]() az elektródtól való távolság.
Az elektródtól távolodva a sűrűségek a megfelelő tömbfázisbeli értékekhez tartanak (
az elektródtól való távolság.
Az elektródtól távolodva a sűrűségek a megfelelő tömbfázisbeli értékekhez tartanak (
![]() ha
ha
![]() ).
).
A kettő különbsége adja a töltéssűrűséget 1:1 elektrolit esetén. Általánosan:
![]() . A töltéssűrűség a fal mellett pozitív és az elektródtól távolodva nullához tart. Ezt a réteget nevezik diffúz rétegnek.
. A töltéssűrűség a fal mellett pozitív és az elektródtól távolodva nullához tart. Ezt a réteget nevezik diffúz rétegnek.
A diffúz rétegben levő töltés pontosan ellensúlyozza az elektródon levő töltést. Az elektródon lévő töltések rétege és a diffúz rétegben levő töltések együtt alkotják a kettősréteget. Ez tulajdonképpen egy dipólréteg, ami egy potenciálugrást létesít a tömbfázishoz viszonyítva. Az elektród felületének potenciálját nevezzük elektródpotenciálnak. Célunk ennek számítása. A tömbfázis elektromosan semleges, ezért átlagos elektromos potenciálja zérus.